由单纯疱疹病毒1型(HSV-1)感染引起的单纯疱疹病毒性角膜炎(HSK)是世界范围内单侧角膜失明的主要原因。据估计,每年有150万例HSK病例发生,其中4万例发展为严重视力障碍。三叉神经节(TG)是HSV-1在原发性急性角膜感染后在宿主中建立终生潜伏的地方,TG神经元中潜伏的HSV-1会重新激活导致反复感染。
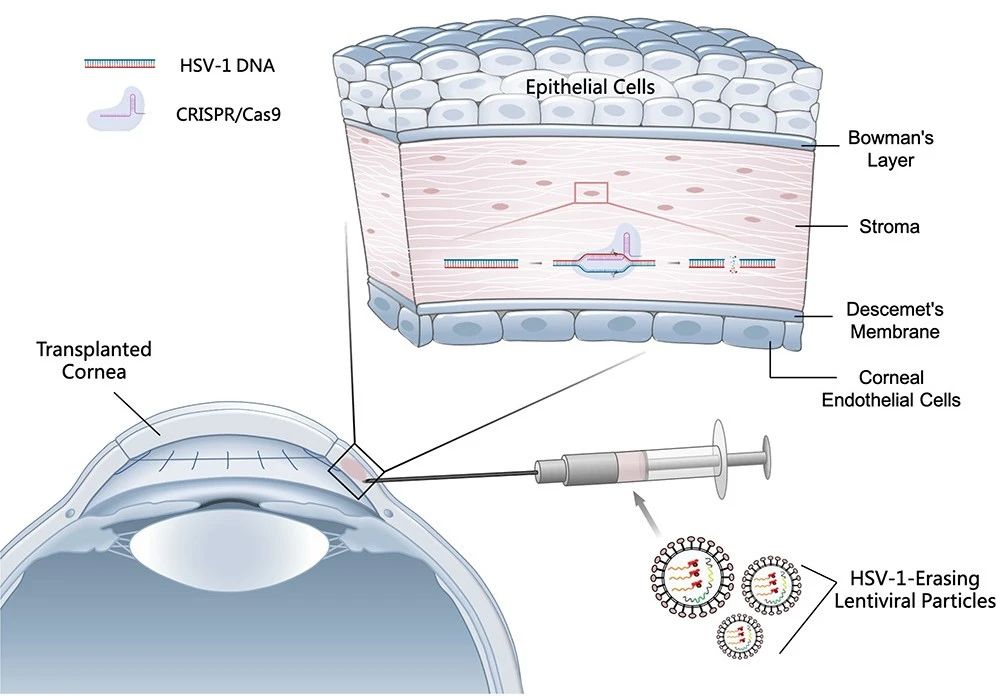
2021年5月,复旦大学附属眼耳鼻喉科医院洪佳旭主任医师和上海交通大学系统生物医学研究院蔡宇伽研究员开发了名为HELP的瞬时靶向基因编辑技术实现了小鼠病毒性角膜炎的完全治愈【1】。HELP技术使用类病毒载体(VLP),以mRNA的形式递送CRISPR-Cas9基因编辑工具,使得Cas9酶在体内停留时间很短,可更大程度地降低脱靶风险、减少免疫反应。并将该技术推进到了临床试验阶段。
2023年8月31日,洪佳旭主任医师、蔡宇伽研究员作为共同通讯作者,在 Molecular Therapy 期刊上发表了题为:In Vivo CRISPR Gene Editing in Patients with Herpes Stromal Keratitis 的研究论文。
该研究对3名伴有急性角膜穿孔的严重难治性单纯疱疹病毒性角膜炎(HSK)患者进行了HELP治疗联合角膜移植,并进行了平均18个月的随访。结果显示,3名患者的未发生HSV-1复发,且没有检测到CRISPR诱导的脱靶效应,也未出现全身性不良事件。
这些初步临床结果表明,HELP有望成为一种全新的体内抗病毒疗法,助力体内基因编辑治疗时代的真正到来,为无药可治、有药难治的遗传性、获得性及感染性疾病的患者带来新的希望。

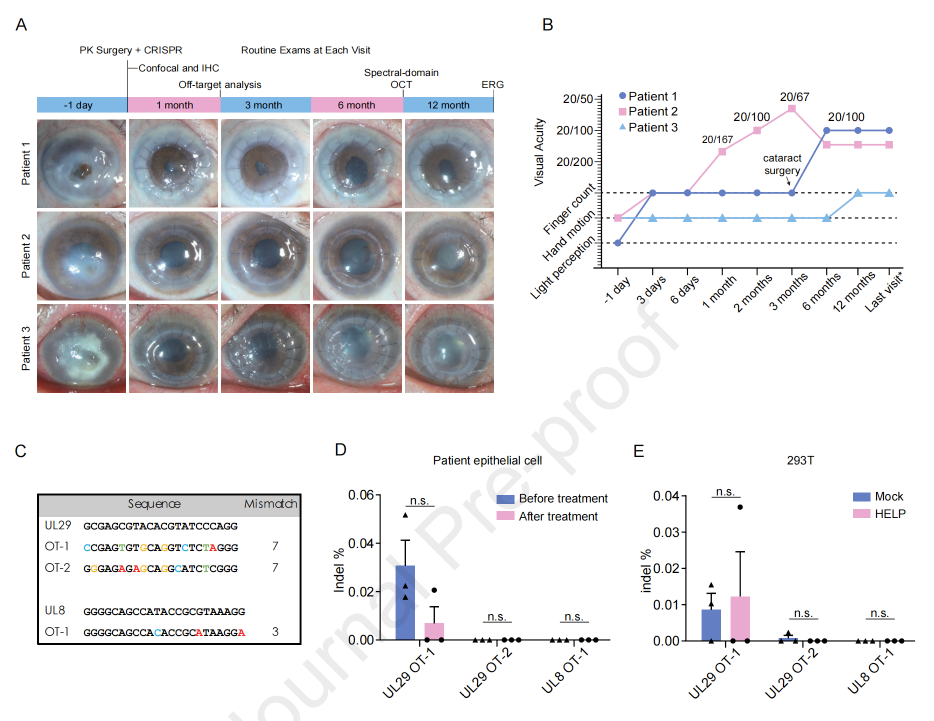
这些初步临床结果表明,HELP可能是限制人类角膜中HSV-1复制的有效策略,且无明显的CRISPR相关副作用,具有可接受的安全性。该疗法在未来还有望将治疗范围扩大到较轻的单纯疱疹病毒性角膜炎(HSK)患者,以防止他们发展为难治性HSK以及发生角膜穿孔并发症。总的来说,这项研究为体内CRISPR基因编辑作为潜在的抗病毒策略提供了临床概念验证。
https://doi.org/10.1016/j.ymthe.2023.08.021













